Ophtalmologie
Publié le 29 sep 2020Lecture 20 min
Deux urgences rares chez l’enfant : cataracte et glaucome - Défis diagnostiques et thérapeutiques
Emmanuel BUI QUOC, Service d’ophtalmologie, hôpital universitaire Robert Debré, Paris
Cataracte et glaucome congénitaux ne sont pas des pathologies obligatoirement congénitales. L’enfant ne naît pas toujours avec le cristallin opacifié ou une hypertonie oculaire, mais avec l’anomalie acquise ou innée qui conduit à la pathologie et dont le traitement chirurgical est une urgence thérapeutique pour préserver le pronostic fonctionnel le meilleur possible et éviter la malvoyance ou la cécité. Le traitement initial conditionne la vie de l’enfant, qui pourra être normale dans le meilleur des cas, mais parfois handicapée par les séquelles cécitantes de sa maladie oculaire.
Cataracte de l’enfant
Histoire
Jadis les enfants présentant une cataracte congénitale étaient tous « amblyopes, strabiques et nystagmiques », disait un de mes maîtres... Ceci était vrai en cas de cataracte unilatérale, l’œil atteint (non opéré car c’était inutile) étant malvoyant, ainsi qu’en cas de cataracte bilatérale opéré, sans implant, avec les consé- quences optiques et parfois tensionnelles de l’aphaquie.
L’implantation précoce et la prise en charge énergique de l’amblyopie nous obligent à un résultat fonctionnel meilleur et presque parfait depuis environ 40 ans. Il est connu depuis des siècles que la cataracte bilatérale doit être opérée le plus tôt possible, Mackenzie l'écrivait dès 1830(1). En revanche, jusqu’aux années 1970 et 1980, il était interdit d’opérer une cataracte unilatérale, Jules François affirmant en 1970(2): « Tout le monde connaît l’inutilité d’opérer la cataracte congénitale unilatérale ». De fait une étude de Prudhommeaux montrait que sur 7 cas unilatéraux opérés, la vision se limitait au mieux à la perception lumineuse. L’amblyopie était la règle à une époque où on ne pratiquait ni implantation, ni extraction manuelle du cristallin(3).
Aujourd’hui, que ce soit dans la cataracte unilatérale ou la cataracte bilatérale, l’objectif d’une vision de plus de 6/10 de chaque œil peut être atteint (limite de la vision légale pour conduire), grâce à une chirurgie précoce et un traitement de l’amblyopie efficace, acharné et long, en sachant que la limite de la malvoyance est 3/10 et la limite de la cécité légale est 1/20.
L'amblyopie
Notre définition de l’amblyopie est celle du rapport de la Société française d’ophtalmologie de 2013 : « L’amblyopie pourrait [...] être définie comme une diminution plus ou moins sévère de la fonction visuelle du fait d’une altération précoce de l’expérience visuelle, le plus souvent asymé- trique, par privation d’une image et/ou perturbation du lien binoculaire par strabisme et/ou anisométropie, avec ou sans anomalie anatomique de l’œil et/ou des voies visuelles retrouvée »(6). D.H. Hubel et T. Wiesel ont décrit depuis les années 1960 la physiologie normale des neurones visuels et l’altération profonde des propriétés neuronales en cas de privation monoculaire (par suture palpébrale) et de strabisme, pendant la période sensible du développement visuel qui dure près d’une décennie chez l’homme. En cas de cataracte, les 3 causes d’amblyopie (figure 1) s’additionnent :
Figure 1. Asymétrie, compétition de l’information sensorielle en provenance des 2 yeux.
Les 3 causes d’amblyopie. Modèle classique pour expliquer l’amblyopie.
– privation monoculaire tant que la cataracte n’est pas opérée ;
– anisométropie dans la cataracte unilatérale après opération précoce, car l’implant est sous-corrigé pour tenir compte de la croissance de la longueur axiale de l’œil, et il existe initialement une hypermétropie unilatérale forte qui régresse ;
– strabisme sensoriel et/ou par absence de binocularité.
Diagnostic
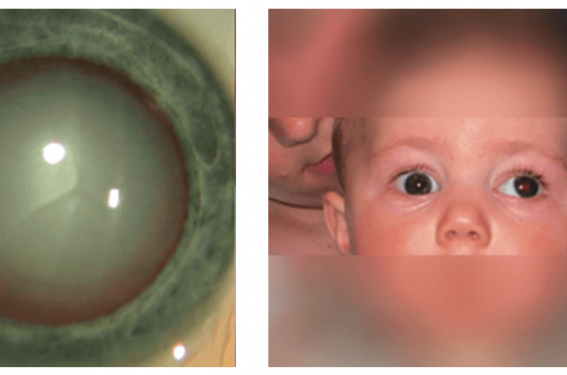
La cataracte n’est pas toujours « congénitale » et peut se manifester secondairement dans les premiers mois ou les premières années de vie. Dans le cas de cataracte unilatérale, il peut exister une leucocorie et/ou un (vrai) strabisme, signe d’amblyopie (figure 2).
Figure 2. Cataracte gauche avec leucocorie et strabisme divergent.
Un examen systématique bien conduit avec dilatation lors de la cycloplégie obligatoire chez l’enfant peut constater l’opacité du cristallin (figure 3).
Figure 3. Cataracte.
Une cataracte bilatérale peut se manifester par une leucocorie, un strabisme, un nystagmus bilatéral et/ou un comportement de mal- voyance, parfois mis en évidence au stade débutant par l’examen systématique.
Épidémiologie
L’incidence dans la population générale est variable selon les études, elle est estimée entre 2,3 et 14 pour 10 000 naissances. L’incidence globale est évaluée à 6 pour 10 000 naissances selon une étude européenne collaborative portant sur 1 832 857 naissances(7). Au regard des 800 000 naissances par an en France, cela correspondrait à 480 cas par an et par classe d’âge de cataracte chez des enfants de de moins de 2 ans. Dans un tiers des cas, la pathologie est bilatérale.
La fréquence de la cécité (acuité visuelle ou AV < 3/60 = 1/20) liée à la cataracte de l’ordre de 0,1 à 0,4 cas pour 10 000 enfants dans les pays occidentaux(8). Les populations à risque sont les nouveau-nés de faible âge gestationnel ou de faible poids de naissance, ceux ayant présenté une anoxie périnatale ou une infection anté- ou néonatale (toxoplasmose, infections virales, notamment à cytomégalovirus), et les enfants avec antécédents familiaux ou porteurs d’anomalies chromosomiques (trisomie 21, par exemple).
Bilan
Le bilan ophtalmologique recherche une dysgénésie associée, s’assure de l’intégrité du segment postérieur (échographie B), fait le calcul de l’implant par mesure de la kératométrie (puissance de la cornée) et évalue la longueur axiale de l’œil.
Le bilan systémique peut rechercher les étiologies de la cataracte congénitale qui sont multiples (tableau 1) :
– héréditaire autosomique dominante/récessive/liée à l’X ;
– syndrome de Lowe, amino-acidurie, etc. ;
– maladies métaboliques : galactosémie (qui se traite par régime +++) ;
– maladie de Wilson après 20 ans ;
– xanthomatose cérébro-tendi- neuse après 10 ans ;
– maladies mitochondriales ;
– infections ;
– cataractes associées à des anomalies chromosomiques : T21, 18, 13 ; délétions (il existe dans ces cas des anomalies associées « évidentes »).
En pratique, toutes les causes ne sont pas recherchées car de toutes façons le plus souvent la cataracte. est idiopathique(10). Finalement, il ne faut rechercher que les causes pour lesquelles il y aurait une conséquence thérapeutique immédiate, comme le régime dans la galactosémie, qui se diagnostique par analyse d’urine avant et après prise d’un biberon de lait, pour doser le galactose dans les urines et évaluer l’activité de la galactokinase.
On réalise volontiers une échographie cardiaque préalable à l’opération et à l’anesthésie générale, à la recherche d’une myocardiopathie associée (rare syndrome de Sengers dans un cas bilatéral).
Le bilan de base est reproduit dans le tableau 2 ; il est à orienter et compléter selon le contexte sys- témique et l’examen pédiatrique.
Thérapeutiques en cas de cataracte congénitale
Le meilleur résultat anatomique possible est obtenu par une chirurgie appliquée par un spécialiste. Le meilleur résultat fonctionnel monoculaire est requis lorsque la cataracte est traitée précocement. En cas de cataracte unilatérale précoce (avant 2 ans), il s’agit toutefois d’un « œil de secours » fonctionnel, car la suppression et l’absence de vision binoculaire les deux yeux ouverts, la probléma- tique de l’amblyopie monoculaire et la problématique réfractive font que l’œil sain demeure l’œil dominant. Ceci est variable selon l’âge de la cataracte avec une normalité monoculaire et binoculaire possibles après 5 ans.
La meilleure acuité possible de chaque œil avec isoacuité est recherchée en cas de cataracte bilatérale, même si la vision peut être limitée et ne pas être de 100 %, par amblyopie bilatérale et en cas d’anomalies associées comme une microphtalmie relative bilatérale.
La chirurgie
La chirurgie sous anesthésie générale a pour étapes : micro-incision cornéenne ou sclérocornéenne (2,2 mm), rhexis antérieur, hydratation et aspiration du cristallin, rhexis postérieur avant l’âge de 5 ans, vitrectomie antérieure, mise en place d’un implant hydrophobe monobloc dans le sac ou d'un 3 pièces dans le sulcus(11).
Il faut implanter d’emblée à tout âge si c’est possible et en l’absence de microphtalmie associée (c’est-à-dire si l’œil est assez grand). Il faut sous-corriger le résultat théorique du calcul d’implant, en prenant en compte l’éventuelle microphtalmie associée :
– 0/3 mois : - 40 % ;
– 3/6 mois : - 30 % ;
– 6/12 mois : - 25 % ;
– 12/24 mois : - 20 % ;
– 24/36 mois : - 10 %.
On ne fait plus de sous-correction après 4 ans.
L’objectif est de rendre l’œil hypermétrope au début (mais pas trop) pour ne pas le rendre trop myope in fine.
L’implant est monofocal avant 5 ans, possiblement multifocal après.
Il faut opérer dès le diagnostic posé. La règle d’intervenir à 6 semaines pour une cataracte unilatérale et à 3 mois pour une cataracte bilatérale est inepte.
Il faut multiplier les examens sous anesthésie : à 1 mois, 3 mois puis tous les 6 mois jusqu’à 3 à 4 ans, afin de détecter et opérer une cataracte secondaire, un glaucome, faire des réfractions précises. Ceci doit être expliquée car c’est astreignant pour les parents, en plus des consultations de suivi.
Traitement de l’amblyopie et suivi
La prise en charge de l’amblyopie « organique » liée à une cataracte « congénitale » est spécifique et assurée par le chirurgien, elle ne doit pas être déléguée. Le traitement optique requiert de multiplier les réfractions et changer les lunettes aussi souvent que nécessaire.
Le traitement de l’amblyopie repose sur l’occlusion sur peau. À l’âge préverbal, il s’agit d’un traitement préventif, à appliquer au mieux 2/3 du temps d’éveil jusqu’à l’âge verbal en cas de cataracte unilatérale, et à adapter ensuite. À partir de 2 ans 1⁄2 - 3 ans, il faut tenir compte de l’acuité visuelle et de la scolarité, et l’indiquer environ la moitié du temps d’éveil répartis sur la journée ou la semaine. À partir de 6 ans, on peut faire l’occlusion le week-end ou proposer une surcorrection optique. Le traitement se prolonge jusqu’à plus de 10 ans.
En cas de cataracte bilatérale, il faut faire une occlusion alternée ou une pénalisation alternée (comme un traitement de strabisme précoce), puis à partir de l’âge verbal, on adapte selon l’acuité visuelle de chaque œil. Le traitement de l’amblyopie en cas de cataracte congénitale est un traitement spécialisé piloté par le chirurgien.
Les objectifs thérapeutiques sont certes modestes car obtenir plus de 6/10 n’est pas une vision normale, mais ce résultat permet une vie normale et est obtenu chez plus des 2/3 des cas bilatéraux et plus de 50 % des cas unilatéraux.
Le traitement est long, « invasif » (à cause de anesthésies générales itératives) pour un résultat en termes d’acuité visuelle imparfait. Des complications sont possibles : inflammation, glaucome, décollement de rétine, etc.
Ainsi, le traitement chirurgical n’est qu’une petite étape. Le traitement optique précis et renouvelé, ainsi que le traitement de l’amblyopie sont primordiaux, avec des équipements spécifiques comme des lunettes « Telex » ou « Franklin », des verres bifocaux ou progressifs. Le coût de la prise en charge est onéreuse et la Sécurité sociale ne le rembourse pas entièrement, même en «100% » :
– avant 6 ans : autant de lunettes que nécessaires sont remboursées en marquant que la correction a changé, de 6 à 18 ans, c’est une paire par an. Les bases de remboursement sont toutefois minimes :
– verre unifocal : de 12,04 à 46,5 €,
– verre multifocal : de 39,18 à 66,62 €,
– monture : 30,49 € ;
– après 18 ans, le rembourse-ment est dérisoire et, quel que soit l’âge, les mutuelles selon leurs bases tarifaires. Il faut donc rappeler aux parents que la médecine n’est pas gratuite et que les lunettes ne sont pas totalement prises en charge, même en affection longue durée (ALD).
ALD et MDPH
Faut-il faire un protocole de soins 100 % (LD) ? Faut-il faire un certificat MDPH (Maison départementale des personnes handicapées) ?
Est-ce que l’enfant est handicapé ? Le traitement d’une cataracte congénitale est long et requiert des consultations, des hospitalisations (même si seulement ambulatoires) et des déplacements itératifs qui peuvent occasionner des coûts pour les parents. Il est donc légitime de demander une ALD hors liste jusqu’à l’âge de 6 ans. Le protocole de soins est validé par le médecin traitant ou le pédiatre, avec avis du spécialiste et validation du médecin de la Sécurité sociale.
En revanche, le certificat MDPH n’est pas obligatoire car pas toujours nécessaire, et parfois délétère. En cas de handicap, quel qu’il soit, il existe un volet 1 rempli par le médecin habituel de l’enfant (médecin traitant ou pédiatre), qui note les éléments systémiques et, si le handicap est lié à la vision, le volet 2 est rempli par l’ophtalmologiste.
La notion de handicap est complexe.
En cas de cataracte unilatérale, il n’y a pas de handicap obligatoire : la vie et la scolarité de l’enfant peuvent être normales avec un œil qui voit moins bien, et même une cécité légale < 1/20 ou une malvoyance < 3/10, si l’œil sain est normal (même si on ne conseillera pas, par exemple, un métier de pilote). La reconnaissance du handicap peut permettre une petite allocation pour les parents et peut aider à la reconnaissance scolaire, mais là encore, un enfant qui a un œil qui voit moins bien et l’autre normal ne requiert pas d’AVS (auxiliaire de vie scolaire) et l’enseignant doit juste être vigilant. L’enfant doit porter ses lunettes, ne serait-ce que pour une protection mécanique des yeux, et certainement pas les enlever dans la cour d’école. En cas de trouble des apprentissages, on ne doit pas imputer à la cataracte les difficultés qui requièrent peut-être une attention particulière de l’enseignant. Stigmatiser un enfant, le désigner comme handicapé peut avoir des conséquences délétères et le condamner au retrait, à l’échec et à la différence. Pour le traitement de l’amblyopie, ou le traitement par collyre parfois au long cours, il n’est pas question de faire des certificats itératifs non règlementaires ou des autorisations de mettre des gouttes.
En cas de cataracte bilatérale, si la vision est de plus de 6/10 (d’un œil et/ou l’autre), la vie est normale sans handicap.
L’inscription MDPH entraîne des évaluations de l’enfant, avec tout une machine médico-administrative parfois inutile. La prudence est donc requise.
Glaucome de l’enfant
Les glaucomes « congénitaux » entraînent une neuropathie optique compressive, sévère et rare. Leur incidence varie de 1/300 000 à 1/2 500, elle est estimée en Europe occidentale à 1/18 500, soit une cinquantaine de naissances par an en France. Selon l’Organisation mondiale de la santé (OMS), 2 à 6 % de la cécité chez les enfants dans le monde est liée à un glaucome congénital.
Il s’agit d’une urgence diagnostique et thérapeutique, de pronostic moins bon que la cataracte, avec des séquelles anatomiques et fonctionnelles (malvoyance) et réfractives (myopie forte) possiblement handicapantes.
Classification
Le glaucome congénital est une dysgénésie a minima du segment antérieur de l’œil.
Les dysgénésies du segment antérieur de l’œil sont des pathologies multiples aux définitions phénotypiques et génotypiques variables. Le glaucome congénital primitif, classiquement récessif autosomique par atteinte du gène CYP1B1, doit faire rechercher un diagnostic associé en relation avec un glaucome congénital secondaire dysgénésique dominant autosomique avec d’autres gènes impliqués : PAX 6, PITX2, FOXC, etc.
Il existe des diagnostics différentiels, soit innés, soit acquis.
Les glaucomes tardifs de l’enfant et de l’adolescent ont une présentation et une génétique différentes. La classification internationale des glaucomes infantiles est reproduite dans la figure 4.
Figure 4. Classification internationale des glaucomes infantiles.
Physiopathologie
Le segment antérieur de l’œil se forme entre la 3e semaine et le 3e mois de vie embryonnaire. C’est pendant cette période que peuvent survenir :
– un arrêt du développement de l’angle irido-cornéen ;
– une insertion antérieure de l’iris ;
– un épaississement des faisceaux trabéculaires.
Ceci entraîne un obstacle à l’écoulement de l’humeur aqueuse et une augmentation de la pression intra-oculaire, avec agrandissement de la taille de l’œil car le collagène est élastique (jusqu’à l’âge de 2/3 ans postnatal), ainsi qu’un passage de liquide dans la cornée qui s’œdématie et, lorsque le collagène se désorganise, devient opaque.
Le développement de l’œil se fait à partir du système nerveux central, il se forme à partir de l’ectoblaste au 18e jour qui constitue la plaque neurale. Celle-ci s’invagine au 20e jour pour former la gouttière neurale, puis le tube neural, d’où proviennent les 2 vésicules optiques. Ainsi, les anomalies dysgénésiques de l’œil sont des « neurocristopathies », par anomalies de migration et/ou différenciation des cellules.
Le développement du segment antérieur de l’œil et de l’angle étant très précoce, se pose la question d’un éventuel diagnostic prénatal sur des critères anatomiques, alors que la patiente ne connaît pas forcément encore sa grossesse. Celui-ci n’est pas possible car l’échographie n’a pas une résolution suffisante à cet âge gestationnel, ni à 6 mois d’ailleurs, et pas plus que l’IRM pour des glaucomes non majeurs.
Les malformations du segment antérieur de l’œil sont les conséquences d’anomalies du développement et de la maturation, les différents phénotypes dépendant du moment où ces perturbations surviennent dans l’embryogenèse et le développement fœtal. Bien entendu, les caractérisations génotypiques récentes permettent de mieux comprendre les processus pathologiques et de repenser la nosologie des dysgénésies du segment antérieur. Les travaux princeps d’excision graduée des cellules de la crête neurale céphalique chez l’embryon de poulet ont permis la classification des malformations du segment antérieur, selon les anoma- lies des cellules dérivées des crêtes neurales.
• Anomalies de formation
Il existe une cyclopie par formation d’une seule vésicule optique ; c’est une anomalie non isolée associée à d’autres malformations faciales de la ligne médiane.
• Anomalies de migration
Il peut survenir un glaucome congénital primitif ou des dysgénésies du segment antérieur (embryotoxon postérieur, anomalie d’Axenfeld, anomalie de Peters, anomalie de Rieger, sclérocornée, aniridie qui concerne l’ensemble des tissus oculaires).
• Anomalies de prolifération, comme l’atrophie essentielle de l’iris, le syndrome de Chandler, le syndrome de l’iris nævus.
• Anomalies de différenciation, comme la dystrophie postérieure polymorphe de la cornée.
La classification de Hoskins et Shaffer se fait selon une approche plus anatomique, elle distingue :
– le glaucome congénital primitif isolée constituant une trabéculo-dysgénésie isolée ;
– les trabéculo-dysgénésies associées ;
– il existe un glaucome par anomalie du développement ;
– l’embryotoxon postérieur constituant une cornéo-dysgénésie ;
– l’aniridie et l’ectropion congénital de l’épithélium pigmenté constituant une trabéculo-irido-dysgénésie ;
– les anomalies d’Axenfeld, de Rieger ou de Peters constituant les trabéculo-cornéo-irido-dysgénésies.
Génétique
Il existe un large spectre phéno-ypique du glaucome secondaire, avec un diagnostic difficile, et parfois des pathologies classées comme glaucome congénital primaire avec des variants des gènes FOXC1 ou PITX2, qui sont habituellement associés au syndrome d’Axenfeld-Rieger. On révise parfois un diagnostic de glaucome congénital primaire en glaucome secondaire dysgénésique, liés à des variants de FOXC1 autosomiques dominants. Il faut être prudent sur le conseil génétique, le diagnostic par séquençage est opportun, mais parfois complexe (coûts).
Un rôle des variants FOXC2 et PITX2 comme facteur modifiant a été mis en évidence dans le glaucome congénital primaire par atteinte de CYPIB1. Ainsi, un séquençage ADN dans une cohorte de 133 familles avec glaucome congénital primaire a montré 6,0 % de porteurs de 4 variants rares de FOXC2 à l’état hétérozygote. L’analyse des variants de FOXC2 et PITX2 dans un groupe de 25 cas de glaucome congénital primaire avec génotype variants de CYP1B1 a montré une fréquence élevée (8 %) de variants de PITX2 hétérozygotes et rares. Il existe un éventuel héritage oligogénique non mendélien impliquant FOXC2 ou PITX2 et CYP1B1, et un rôle modificateur des variants de FOXC1, FOXC2, PITX2 sur l’âge de début et la gravité du glaucome congénital associé au CYP1B1.
Les combinaisons d’altérations modérées de gènes impliqués dans le développement du segment antérieur de l’œil peuvent entraîner une perturbation cliniquement significative du développement du trabéculum, et donc un glaucome.
Le diagnostic uniquement phénotypique du glaucome congénital primaire sans anomalie systémique ou oculaire associée doit être prudent.
Diagnostic et traitement du glaucome congénital isolé primitif
Dans le glaucome congénital primaire, il existerait un retard de maturation du trabéculum, avec persistance d’une membrane (dite) de Barkan qui n’aurait pas disparu assez tôt dans l’angle et faisant obstacle à l’écoulement de l’humeur aqueuse.
Quel que soit le mécanisme réel, il existe avant 2 ans une buphtalmie (œil trop gros), un œdème de cornée (donnant un reflet brillant, voire une opacité) et une excavation papillaire au fond d’œil. L’atteinte peut être uni- ou bilatérale (figure 5).
Figure 5. Glaucome bilatéral asymétrique majoré à gauche
Le diagnostic peut être « congénital » à la naissance ou d’apparition retardée (même si l’anomalie est congénitale).
Le diagnostic positif se fait à l’examen sous anesthésie générale, immédiatement avant l’éventuelle chirurgie, avec objectivation de l’augmentation de la longueur axiale par rapport à la normale (17 mm à la naissance ; 18,5 mm à6mois;20mm à 1an ; 23mm à 10 ans), de l’œdème de cornée par pachymétrie (normale entre 500 et 600 μm) et l’augmentation du diamètre cornéen (10 mm à la naissance ; 11,5 mm à 1 an). La mesure du tonus oculaire lui-même est difficile et imprécise sur une cornée œdémateuse et flasque.
Le glaucome congénital est une pathologie rare survenant dans la 1re ou 2e année de vie, bilatérale, dans trois quarts des cas. Elle est grave, cécitante, c’est une urgence chirurgicale.
Les circonstances de découverte sont évidentes ou pas :
– évidentes en cas de forme précoce sévère, avec blocage angulaire total : l’hypertonie oculaire entraîne une distension de la paroi externe avec atteinte du nerf optique, le tableau est alarmant ;
– moins évidentes, dans une forme infantile avec blocage angulaire modéré : le tonus oculaire est moins élevé, le tableau initial moins alarmant avec installation des signes de façon lentement progressive, sans contexte évocateur, ni signe franc (mégalocornée symétrique modérée, peu de photophobie, etc.). Seul un examen sous anesthésie générale redresse le diagnostic, évalue l’état initial et l’éventuelle nécessité chirurgicale.
L’équipe marseillaise a montré que les pédiatres adressent l’enfant dans plus de la moitié des cas pour cette suspicion de glaucome congénital (figure 6).
Figure 6. Qui adresse l'enfant au centre de référence ?
Le traitement est une chirurgie filtrante d’emblée, souvent à répéter, avec des examens sous anesthésie générale itératifs, une surveillance et un suivi toute la vie. La question de l’amblyopie est la même que dans la cataracte, aggravée par l’amétropie forte possible (myopie forte car l’œil est trop long). Parfois, voire souvent, le traitement n’est pas efficace avec des récidives précoces ou tardives, conduisant malgré les opérations multiples, le cycloaffaiblissement laser et les valves mécaniques, à la malvoyance ou à la cécité(12).
ALD et MDH
À la différence de la cataracte, on est souvent amené à envisager le handicap.
En réalité, deux situations existent :
– dans les formes de bon pronostic, il n’y a qu’un retard de maturation fugace, et la prise en charge initiale aide à passer un cap. L’œil se normalise totalement et le glaucome est guéri, pouvant laisser une myopie séquellaire, mais pas de neuropathie optique, car les cellules ganglionnaires peu atteintes se régénèrent ;
– dans les formes plus sévères, l’angle n’est jamais normal, et l’équilibre est précaire entre sécrétion et excrétion d’humeur aqueuse, avec possible traitement médical par collyre au long cour, chirurgies itératives. Le déséquilibre peut survenir et parfois le traitement n’est plus efficace, sans évoquer les complications cécitantes de la chirurgie (hypotonie trop forte, hémorragie intraoculaire, etc.).
En cas de malvoyance < 3/10, la reconnaissance du handicap est obligatoire. Une scolarité normale peut toutefois être possible même à des acuités visuelles basses, avec ou sans adaptation.
La prise en charge ALD est justifiée toute la vie dans les formes non guéries.
Glaucome de l’enfant et de l’adolescent et glaucome juvénile
Le glaucome juvénile à angle ouvert est une maladie rare, grave et potentiellement cécitante. Il n’y a pas d’atteinte systémique associée. Il concerne l’enfant de 3 à 18 ans et représente 6 % des glaucomes primitifs. Son incidence est de 0,32/100 000 des patients de moins de 20 ans.
La maladie est bilatérale et souvent asymétrique.
La transmission est génétique dominante avec nécessité de dépistage : les loci génétiques sont GLC1A, GLC1J, GLC1K, GLC1M, GLC1N. Seul le gène GLC1 A qui code pour la myoci- line a été identifié. On estime que plus de 20 % des patients ont une mutation du gène myociline (TIGR) sur ce locus GLC1A du chromosome 1q23.
Le glaucome juvénile est plus fré- quent chez les sujets mélanodermes.
La physiopathologie est méconnue, mais on retrouve un épaississement du trabéculum en gonioscopie avec possible insertion antérieure de l’iris.
La maladie est asymptomatique, la myopie possible mais inconstante ; en l’absence d’histoire familiale, la découverte est fortuite d’une hypertonie oculaire, avec ou sans déficit d’emblée du champ visuel ; le traitement est chirurgical d’emblée.
• Glaucomes systémiques
Les différents types de glaucomes systémiques sont cités dans la figure 7 : glaucomes systémiques.
Figure 7. Causes de glaucome sytémique
Conclusions : cataracte et glaucome, des cécités évitables
Cataracte et glaucome sont des pathologies rares de l’enfant, mais potentiellement cécitantes et donc de diagnostic précis, urgent pour une prise en charge rapide. Elles sont dites « congénitales » mais surviennent de façon souvent retardée dans les deux premières années de la vie. Devant un reflet anormal dans l’œil ou un strabisme vrai, c’est-à-dire une réelle déviation des yeux l’un par rapport à l’autre, un examen ophtalmologique avec dilatation, cycloplégie et fond d’œil est requis rapidement.
L’absence de parallélisme n’est pas toujours facile à déterminer à l’âge préverbal, car en cas de « suspicion de strabisme » avant 1an, 9 cas sur 10 sont de faux strabisme, par épicanthus (œil recouvert en interne par les plis de paupières), et 1 cas sur 10 un vrai strabisme, le plus souvent strabologique, parfois par anomalie organique comme une cataracte (strabisme sensoriel). Dans tous les cas, un examen ophtalmologique est requis dans le doute, qui peut d’ailleurs mettre en évidence un épicanthus et un strabisme.
Un nystagmus de malvoyance peut être lié à une mauvaise vision des deux yeux, une cataracte pouvant être la cause. Le glaucome de l’enfant entraîne une hypertonie qui est à l’origine d’une neuropathie optique. À la surface, on observe un œil trop gros et une cornée œdématiée et non transparente.
La chirurgie est obligatoire dans les semaines qui suivent le diagnostic pour la cataracte, dans les jours qui le suivent celui de glaucome. Après traitement chirurgical, médical et optique, la prise en charge préventive et thérapeutique de l’amblyopie est obligatoire, afin de traiter les conséquences centrales corticales de l’altération précoce de l’expérience visuelle qui perturbe la maturation des neurones visuels. Ceux-ci sont rééquilibrés par occlusion d’un œil et/ou de l’autre selon la symétrie ou l’asymétrie de la pathologie.
Glaucome et cataracte de l’enfant sont donc à la fois de urgences chirurgicales et des pathologies « chroniques » dont la prise en charge est longue, avec des consultations et des examens sous anesthésie générale itératifs requis pendant la première décennie de la vie.
Parfois, si la malvoyance s’est installée, la prise en charge du handicap est nécessaire, plus dans le glaucome que dans la cataracte, dont le pronostic fonctionnel visuel est maintenant le plus souvent bon, avec vision > 6/10 dans deux tiers des cas bilatéraux et dans la moitié des cas unilatéraux.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :