Publié le 28 aoû 2006Lecture 11 min
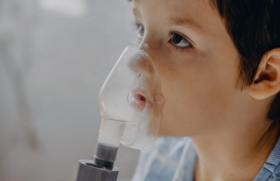
Pleurésies purulentes de l’enfant : Prise en charge actuelle
J. de Blic - Hôpital Necker-Enfants malades, Paris
On assiste actuellement à une augmentation des pleurésies purulentes chez l’enfant dont les causes ne sont pas bien déterminées. Ces pathologies sont également plus sévères, avec des durées d’hospitalisation plus longues.
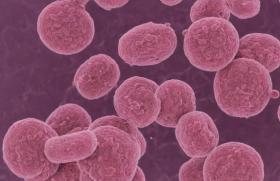
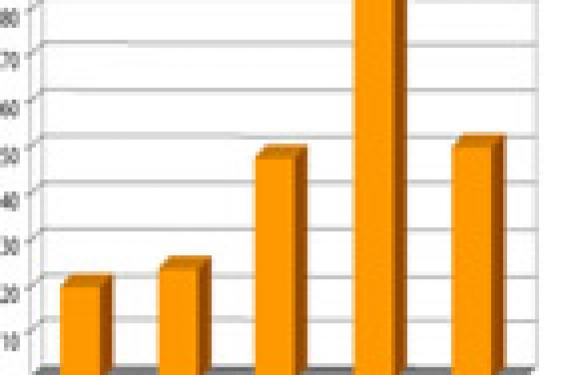
Figure 1. Hospitalisations à Houston (Texas) en raison d’une pleurésie purulente de 1990 à 2002 (d’après Schultz, Pediatrics 2004) Depuis la fin des années 1990, les pédiatres hospitaliers observent en France une augmentation importante et préoccupante du nombre de pleurésies purulentes chez l’enfant. Complications d’une pneumonie bactérienne, les pleurésies purulentes de 2004 ont été aussi plus sévères, avec des durées d’hospitalisation prolongées, souvent 2 à 3 semaines. Si l’antibiothérapie ne pose pas de problèmes d’indication, en revanche, la prise en charge de l’épanchement reste nettement hétérogène d’un centre à l’autre, allant de la simple ponction à la décortication pleurale. Une pathologie de plus en plus fréquente Entre 1995 et 2003, l’incidence des pleurésies purulentes a été multipliée en France par 4 ou 5. Cette augmentation semble suivre, de façon décalée, ce qui a été observé aux États-Unis depuis le début des années 1990. Ainsi, une étude épidémiologique américaine dans l’État de l’Utah, entre 1993 et 1999, a montré que le pourcentage de pleurésies purulentes par rapport aux pneumopathies communautaires est passé de 13 % en 1994 à 41 % en 1997, soit une augmentation de 1 cas pour 100 000 à 5 cas pour 100 000 dans la même période (figure 1). « En France, entre 1995 et 2003, l’incidence des pleurésies purulentes a été multipliée par 4 ou 5. » Les germes en cause Sur le plan microbactériologique, Streptococcus pneumoniae est largement prédominant, devant Staphylococcus aureus et les autres germes anaérobies (Streptococcus viridans et milleri, Escherichia coli, Pseudomonas aeruginosa, Klebsiella pneumoniae). Les germes anaérobies sont exceptionnels et Haemophilus influenzae a quasiment disparu depuis la vaccination systématique. Après un pic pendant les années 1999-2000, il a été noté une diminution progressive, sans pour autant revenir au niveau antérieur. Cette diminution des pleurésies purulentes observée aux États-Unis a coïncidé chronologiquement, avec un décalage de 1 ou 2 ans, avec la généralisation de la vaccination anti-pneumococcique par vaccin heptavalent. L’étude des germes retrouvés durant cette période a montré une diminution du Streptococcus pneumoniae, passant de 66 à 27 % des germes retrouvés, et, parallèlement, une augmentation du Staphylococcus aureus qui est passé de 18 à 60 % des germes retrouvés. Il est à noter que les trois quarts des staphylocoques aureus étaient méticilline-résistant. Pourquoi cette augmentation ? Plusieurs facteurs ont été invoqués pour expliquer cette augmentation des pleurésies purulentes. Un facteur viral Plusieurs mécanismes pourraient expliquer la relation entre la survenue d’une infection virale et celle d’une infection bactérienne, notamment à Streptococcus pneumoniae : – transmission accrue des souches bactériennes lors des situations épidémiques virales par la projection des gouttelettes de Pflügge ; – augmentation de l’adhésion muqueuse des souches bactériennes pathogènes sous l’influence d’une co-infection virale, à l’origine d’une augmentation de la colonisation rhinopharyngée. La survenue d’une infection systémique étant conditionnée par un portage préalable, une augmentation du portage pourrait être à l’origine d’une augmentation du risque brut de la survenue d’infections. Enfin, une coopération non spécifique virus-bactérie pourrait être susceptible d’augmenter le potentiel invasif des pneumocoques. La conjonction de l’altération des fonctions phagocytaires antibactériennes des leucocytes et de la destruction de l’épithélium cilié peut faire le lit de l’infection bactérienne. Un facteur bactérien Si les bactériémies sont plus fréquentes en cas de pleurésie purulente avec des pneumocoques de sensibilité diminuée aux pénicillines, il n’y a pas d’influence sur la durée de l’hyperthermie, de l’hypoxie, du drainage pleural ou de l’hospitalisation. Certaines équipes ont trouvé que le sérotypes 1 serait plus souvent en cause en cas d’empyème, mais il ne s’agit pas d’un sérotype très répandu. Il pourrait s’agir d’une modification de la pathogénicité des souches des Streptococcus pneumoniae. Cependant, le sérotypage des souches isolées dans les pleurésies purulentes a montré que les sérotypes étaient variés et qu’il ne s’agissait probablement pas d’un phénomène oligoclonal ou monoclonal. Figure 2. Pleurésie purulente importante avec opacité de tout l’hémichamp gauche et refoulement médiastinal. Un facteur médicamenteux Plusieurs arguments plaident pour un effet des anti-inflammatoires non stéroïdiens sur la colonisation pharyngée, voire sur la pathogénicité bactérienne. En effet, les AINS pourraient avoir une action inhibitrice de l’adhérence des leucocytes de la phagocytose et de la bactéricidie in vitro, et certains inhibiteurs de la cyclo-oxygénase pourraient induire une augmentation de la production de cytokines, tel le TNF a. A B C Figure 3. Pleuropneumopathie droite. Hémoculture positive à pneumocoque. Épanchement de moyenne abondance (A). Pneumopathie excavée du segment apical du lobe inférieur droit en TDM (B et C). Par ailleurs, d’un point de vue épidémiologique, il a été observé que la prise d’AINS au cours des varicelles pouvait être associée à un risque accru de survenue de fasciites nécrosantes. En ce qui concerne plus spécifiquement les pleurésies purulentes, le travail qui a été réalisé dans l’Utah a montré que l’exposition aux AINS dans les jours précédents était significativement plus fréquente chez les enfants atteints de pleurésie purulente que chez les enfants atteints de pneumopathie bactérienne non compliquée. Cependant, il s’agit d’une étude rétrospective, avec un certain nombre de limites méthodologiques, telle l’éventuelle prise plus fréquente d’AINS, en raison d’un début plus fébrile, chez un enfant atteint de pleurésie purulente que chez les témoins atteints de pneumopathie aiguë bactérienne non compliquée. En tout état de cause, cette augmentation actuelle des pleurésies purulentes, avec des formes qui sont par ailleurs plus sévères, n’a pas d’explication claire et nécessite la mise en commun, de façon prospective, de l’ensemble des pleurésies purulentes observées. La ponction pleurale, indispensable mais encore insuffisamment réalisée Reconnaître l’épanchement L’épanchement pleural, habituellement associé à une pneumopathie aiguë, est évoqué à l’examen clinique (matité avec diminution du murmure vésiculaire et des vibrations vocales), mais plus souvent en fait sur la radiographie de thorax. Selon l’importance de l’épanchement, l’opacité effacera le cul-de-sac costodiaphragmatique, se limitera à une ligne bordante, occupera la moitié d’un hémichamp avec la classique ligne de Damoiseau, ou tout un hémichamp avec des signes de refoulement médiastinal (figures 2 à 4). Figure 4. Pleuropneumopathie gauche. Épanchement pleural occupant les deux tiers de l’hémithorax gauche (a). En TDM (b), le lobe inférieur gauche apparaît atélectasié de façon passive. Examen du liquide pleural La ponction pleurale doit suivre la mise en évidence radiologique de l’épanchement. Outre le fait qu’elle peut identifier le germe en cause, elle confirme le diagnostic de pleurésie purulente et en précise le stade évolutif. Le diagnostic repose sur l’aspect purulent du liquide et sur ses caractéristiques biochimiques selon les critères de Light : – pH £ 7,2 ; – protides : > 30 g/l ; – glucose : £ 40 mg/dl ; – lactico-déshydrogénase (LDH) > 1 000 UI/l ; – prédominance de polynucléaires neutrophiles. La documentation bactérienne repose sur l’identification bactérienne, généralement dans le liquide de ponction (examen direct ou culture), soit encore par la mise en évidence d’antigènes solubles, ou par PCR pour le Streptocoque. Cette ponction pleurale est indispensable mais actuellement encore sous-réalisée. Il s’agit cependant d’un geste technique relativement simple qui peut être réalisé sans danger au lit de l’enfant. Prise en charge de l’épanchement Si l’antibiothérapie intraveineuse ne se discute pas, la prise en charge de l’épanchement n’est pas consensuelle. Les antibiotiques L’antibiothérapie repose sur le céfotaxime ou la ceftriaxone IV seuls chez l’enfant de plus de 2 ans, et sur l’association de céfotaxime ou ceftriaxone et de fosfomycine chez l’enfant de moins de 2 ans. L’antibiothérapie est généralement intraveineuse pendant 15 jours, avec un relais per os par amoxicilline ± acide clavulanique pendant 4 semaines. Principes thérapeutiques La prise en charge de l’épanchement pleural fait appel aux ponctions répétées, au drainage, aux fibrinolytiques, à la thoracoscopie et à la thoracotomie. D’un point de vue purement théorique, aux 3 phases de la pleurésie purulente devraient correspondre 3 attitudes thérapeutiques. Lors de la phase exsudative,, qui correspond à un liquide fluide avec peu de cellules, un drainage simple devrait suffire. À la phase fibrino-purulente, riche en polynucléaires et en fibrine et aboutissant à des cloisonnements, des fibrinolytiques pourraient être utiles, de même que la libération des brides sous thoracoscopie. Enfin, lors de la phase organisée avec formation d’une couenne engainant le poumon, la thoracotomie deviendrait indispensable. Apport de l’imagerie La conduite thérapeutique peut (doit) s’aider de l’imagerie. L’échographie est la méthode de base. Elle précise l’abondance de l’épanchement et son échogénicité. Elle permet de localiser un cloisonnement débutant et de guider une ponction ou un drainage. La tomodensitométrie (TDM) donne des images plus précises. Elle localise plus exactement les poches pleurales et précise mieux que l’échographie l’atteinte parenchymateuse sous-jacente en distinguant un abcès pulmonaire d’un empyème. C’est l’examen de choix quand l’évolution n’est pas probante, pour décider d’une thoracoscopie ou d’une thoracotomie. Proposition pratique Une métaanalyse récente des différentes prises en charge de l’épanchement des pleurésies purulentes montre l’absence totale de consensus. Une seule étude sur les 44 analysées est prospective. Cette étude a comparé un drainage versus des ponctions pleurales itératives (une à quatre). Elle a montré que s’il n’existait pas de déviation médiastinale importante, les ponctions itératives étaient aussi efficaces que le drainage, sans différence pour la durée de la fièvre ou de l’hospitalisation. L’essentiel des études est donc rétrospectif, avec bon nombre de biais méthodologiques. Mais la conclusion principale de ces études qui comparent le drainage seul, le drainage plus les fibrinolytiques, la thoracoscopie et la thoracotomie, est que la durée d’hospitalisation est plus courte en cas de thoracoscopie précoce ou de thoracotomie qu’en cas de drainage seul. La prise en charge de l’épanchement pleural pourrait donc être proposée selon la façon illustrée par la figure 5. • En cas d’épanchement pleural faible confirmé par échographie, une antibiothérapie seule est suffisante. Il s’agit alors d’un épanchement parapneumonique qui disparaîtra avec la pneumonie. • Si l’épanchement pleural est abondant, la ponction est indispensable et permet de retenir 3 situations : – le liquide est clair, les critères biochimiques sont favorables et il n’y a pas de germe au direct : une simple surveillance sous antibiotiques doit suffire mais peut nécessiter, secondairement, un drainage en cas de mauvaise tolérance ; – le liquide est clair ou trouble avec des critères biochimiques intermédiaires : le drainage n’est alors proposé qu’en cas de mauvaise tolérance ; – il s’agit d’une pleurésie ayant les caractères de la pleurésie purulente. La prise en charge de l’épanchement va dépendre de la tolérance, des données de l’échographie et de la tomodensitométrie (importance de la pneumonie, caractère cloisonné ou non cloisonné) et, surtout, des habitudes et des possibilités de l’équipe médico-chirurgicale. Figure 5. Schéma de prise en charge des pleuropneumopathies de l’enfant. Des séquelles exceptionnelles Malgré l’importance du syndrome infectieux et des images radiologiques parfois impressionnantes, l’évolution à long terme des pleurésies purulentes ou des pleuropneumopathies purulentes de l’enfant est très favorable, avec une normalisation radiologique le plus souvent complète et des fonctions pulmonaires normales à distance. La décortication reste absolument exceptionnelle chez l’enfant. En l’absence d’atteinte plurisystémique, il n’est pas nécessaire de rechercher un déficit immunitaire. Au total, la prise en charge de l’épanchement n’est actuellement pas codifiée, mais quelle qu’elle soit, le pronostic à long terme reste bon.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :