Publié le 29 oct 2012Lecture 9 min
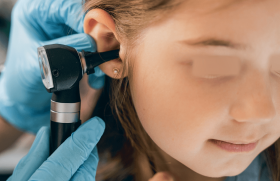
Une gêne à la mastication
D. ARMENGAUD, CHI de Poissy/Saint-Germain-en-Laye

Louis, âgé de 6 ans ½, est adressé par son médecin traitant en raison de difficultés à la mastication associées à une voix « nasonnée » depuis 4-5 jours. Il est revu 4 jours plus tard avec une aggravation d’un ptosis bilatéral.
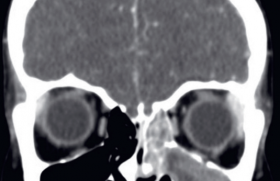
Histoire clinique L’enfant, suivi régulièrement, n’avait jamais posé le moindre problème, ni présenté de manifestation de ce type. Les difficultés à la mastication et la voix nasonnée sont survenues dans un contexte banal de rhinopharyngite modérément fébrile. Inquiet face à ces manifestations, une tomodensitométrie crânienne a été demandée en ville, qui s’est avérée normale. La NFS montre : – Hb : 13,1 g/dl ; – GR : 4 570 000 mm3 ; VGM : 82 μ3 ; – GB : 3 000/mm3 (PNN : 8 % ; Eo : 10 % ; baso : 0 % ; lympho : 64 % ; mono 18 %) ; – plaquettes : 386 000/mm3. Il s’agit d’un premier enfant sans antécédents particuliers, hormis une mononucléose infectieuse à l’âge de 3 ans d’évolution simple. L’interrogatoire ne retrouve pas la notion de traumatisme, mais une piqûre de moustique au niveau du visage 3 semaines auparavant sans érythème, ni éruption. L’enfant est en bon état général avec, cependant, un certain degré d’asthénie. Il est apyrétique (36 °C), avec une bonne hémodynamique (pression artérielle : 99/68 mmHg ; FC : 84/min). Il pèse 23 kg (+1 DS) pour une taille de 118 cm (+1 DS). L’auscultation cardio-pulmonaire est normale, il n’y a pas de dyspnée, pas de toux. L’examen ORL est normal, en dehors d’une rhinite banale sans caractère obstructif ni hypertrophie des amygdales, qui sont saines. Il n’y a pas de masse rétropharyngée visible à l’examen. L’examen neurologique retrouve une force musculaire normale, symétrique, avec des réflexes ostéotendineux présents et symétriques. Il n’y a ni dystonie, ni syndrome pyramidal ou extrapyramidal. L’oculomotricité est normale, ainsi que les réflexes photomoteurs et consensuels présents et symétriques. Il n’y a pas de paralysie faciale, mais Louis se plaint effectivement d’une difficulté d’élocution et à la mastication avec une petite déviation de la mâchoire à l’ouverture de la bouche semblant se majorer plutôt en fin de journée. Il n’y a pas de troubles de déglutition, ni de fausse route. Il n’y a pas de syndrome méningé et la nuque est parfaitement souple et indolore. Un contrôle de NFS et une sérologie de Lyme sont demandés en externe. Il est prévu de revoir l’enfant dans la semaine, mais entre temps, il se présente de nouveau aux urgences 4 jours plus tard en raison d’une majoration de la gêne à la mastication, avec difficulté à finir ses repas, mais aussi à la phonation avec des problèmes d’articulation, et apparition d’un ptosis bilatéral. Figure 1. Radiographie pulmonaire normale (absence de masse médiastinale). Hypothèses diagnostiques Si une gène à la mastication peut être rencontrée occasionnellement chez l’enfant, elle est le plus souvent en rapport avec des phénomènes douloureux, inflammatoires et/ou infectieux (angine, adénopathies, abcès), qui sont ici absents et ne peuvent expliquer les signes présentés par ce garçon. Dans un contexte de ce type, le premier diagnostic évoqué est celui d’une paralysie faciale, périphérique, qui prédomine sur le nerf facial inférieur et s’accompagne souvent d’une déviation de la commissure labiale. On parle de paralysie faciale « a frigore » ou essentielle, par élimination des autres causes, dont la plus fréquente est certainement la maladie de Lyme. Encore faut-il que le contexte s’y prête : antécédent de piqûre (morsure de) de tique au niveau de la tête ou du cou (les enfants étant plus petits que les adultes, les morsures siègent plus souvent au niveau du tronc ou des membres inférieurs), ici absent, tout comme la réaction méningée associée. La sérologie de Lyme demandée reviendra négative. De même, la compression d’un nerf crânien, par un processus tumoral, même en l’absence de signes d’hypertension intracrânienne, est à évoquer. La réalisation d’un scanner (ou d’une TDM récente), avec résultat normal, permet de ne pas envisager ce diagnostic. L’aggravation des signes et notamment l’apparition d’un ptosis permet d’ouvrir un peu plus la discussion sur l’origine possible des symptômes présentés par l’enfant. On peut éliminer un ptosis congénital, le plus souvent unilatéral, banal, bénin et fréquent (60 % des ptosis), qui se révèle en général plus précocement. En revanche, devant un ptosis acquis, plusieurs diagnotics peuvent être évoqués : • un syndrome de Claude Bernard Horner (20 %), associant : – ptosis (il s’agit plutôt d’un défaut de rétraction de la paupière inférieure que d’une paralysie du releveur), qui est également unilatéral ; – myosis ; – énophtalmie ; dont les causes sont très rares chez l’enfant (cancer du poumon chez l’adulte) en dehors d’un traumatisme cervical (chute, sport de combat), ici absent, qui peut être à l’origine d’une dissection de la carotide, qui pourrait être à l’origine du syndrome. • Une dissection carotidienne pourrait tout autant entraîner une paralysie du nerf moteur oculaire commun avec mydriase (III extrinsèque), paralysie de l’accomodation (III intrinsèque), défaut de l’élévation ou de l’abaissement du regard et de l’adduction donnant un strabisme divergent « récent ». Toutes ces causes ont en commun de provoquer un ptosis unilatéral mais s’accompagnant souvent de manifestations douloureuses. Elles ne peuvent donc être retenues ici. En revanche, il faut, malgré leur rareté, évoquer par élimination : – non pas tant un botulisme d’évolution plus rapide après ingestion d’aliments suspects (conserves familiales), avec diplopie par paralysie d’accomodation et sécheresse de la bouche (ici absentes) ; – mais une myasthénie autoimmune, en raison du caractère fluctuant des signes, de leur prédominance vespérale avec fatigabilité progressive au cours de la journée et récupération partielle après le repos de la nuit, qui sont aussi des signes très évocateurs. Sur ces considérations, un test diagnostique à la Prostigmine® (néostigmine 50 μg/kg) sera réalisé et considéré comme positif du fait d’une amélioration rapide, mais fugace, des troubles présentés par l’enfant. Commentaires La myasthénie est une affection qui peut concerner aussi l’enfant. On distingue trois types : – congénitale, extrêmement rare (1/500 000), défaut de la jonction neuromusculaire de transmission autosomique récessive, de révélation anté- ou néonatale, avec une hypotonie majeure et une insuffisance respiratoire aiguë à la naissance ; – néonatale, chez un nouveauné de mère myasthénique par transmission d’anticorps antirécepteur de l’acétylcholine. Les manifestations peuvent être également anténatales (hydramnios, arthrogrypose) ou néonatales (cri faible, insuffisance respiratoire, troubles de la déglutition) et trompeuses si la maladie maternelle n’est pas connue. La régression des troubles se fait en 4 à 6 semaines à mesure de l’élimination des anticorps transmis (dont le suivi des taux a une bonne valeur pronostique) ; – auto-immune, avec une fréquence estimée à 4-6 pour 100 000, avec habituellement une prédominance féminine. Le diagnostic était apporté par l’EMG qui montre, lors de stimulations répétées, une diminution de la réponse motrice (décrément), caractéristique de l’épuisement de la réponse musculaire. Le diagnostic, de manière moins invasive, peut être apporté par la mise en évidence d’auto-anticorps anti-récepteur de l’acétylcholine retrouvés dans 80 % des cas, mais pas toujours au début, ou anti-muSK (récepteur de tyrosine kinase spécifique du muscle). La myasthénie est une maladie de la jonction neuromusculaire associant une raréfaction des récepteurs de l’acétylcholine (proportionnelle à la gravité de la maladie) et une modification (élargissement) de la jonction neuro-musculaire. L’acétylcholine libérée à l’extrémité du motoneurone spinal se fixe sur le récepteur, entraînant une ouverture d’un canal cationique au niveau de la fibre musculaire générant un potentiel électrique. La diminution du nombre de récepteurs ne permet plus d’atteindre le seuil déclenchant la contraction musculaire, surtout si la commande se répète. Le muscle devient de moins en moins apte à se contracter, ce d’autant qu’au fur et à mesure le largage d’acétylcholine diminue. La fatigabilité lors de contractions itératives, ou au cours de la journée, avec une certaine récupération par le repos, est caractéristique. Figure 2. Électromyogramme sous traitement par pyridostigmine : persistance d’un décrément significatif (18 %) caractéristique de la myasthénie, lors des stimulations répétées du nerf cubital. Le facteur déclenchant de la maladie n’est pas connu, tout comme ce qui conduit au maintien du taux des anticorps. Cela doit conduire, notamment chez l’adulte, à la recherche d’un thymome (exceptionnel chez l’enfant) et à procéder à une thymectomie. Le traitement repose sur l’administration d’un anticholinestérasique, qui permet d’augmenter la demi-vie de l’acétylcholine et de palier, pour une part, la diminution des récepteurs. La posologie est à adapter au cas par cas, évoluant entre insuffisance thérapeutique et surdosage. La « crise cholinergique » se traduit par des signes : – muscariniques : douleurs abdominales, nausées, vomissements, hypersalivation, diarrhée, myosis ; – et/ou nicotiniques : crampes, fasciculations musculaires. Ces signes de surdosage sont réversibles sous parasympathicolytiques, c'est-à-dire par de l’atropine qui est systématiquement associée au traitement de fond (elle peut être aussi utilisée par voie sous-cutanée [0,02 mg/kg]). Différents traitements immunomodulateurs (corticoïdes, gammaglobulines) ou immuno-suppresseurs (azathioprine, micophénolate mofétil) sont discutés, surtout chez l’adulte, en cas de réponse insuffisante aux anticholinestérasiques. D’autres voies de recherche sont en cours (récepteur soluble, vaccin, anticorps monoclonal, etc.). Diagnostic positif La recherche d’anticorps antirécepteur de la cholinestérase sera négative, tout comme la recherche d’auto-anticorps antimuSK ou d’autres manifestations d’auto-immunité. • Après contact avec le centre de référence, un traitement par pyridostigmine (Mestinon®) à la posologie de 30 mg x 4/j associé à de la teinture de belladone sera mis en route rapidement devant l’aggravation des signes cliniques (gêne à la déglutition), et permettra une équilibration correcte de cette myasthénie séronégative. • Un EMG sera réalisé quelques semaines plus tard montrant un décrément des potentiels d’action estimé entre 18 et 14 % (figure 2) suffisant pour affirmer le diagnostic, avec une phase de stabilisation en rapport avec le traitement par anticholinestérasique.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :