ORL et Stomatologie
Publié le 21 mai 2014Lecture 14 min
Hypersalivation du jeune enfant
Vincent COULOIGNER*, Julia COHEN LEVY**, *Service d’ORL, Hôpital Necker-Enfants Malades, AP-HP, Université Paris-Descartes, **Cabinet d’orthopédie dento-faciale, Paris
Les hypersalivations peuvent être bénignes, en rapport avec la persistance d’une déglutition primaire et souvent associées à des anomalies de l’occlusion dentaire. Leur prise en charge fait alors appel à de la rééducation ou à un traitement orthodontique. Les hypersialorrhées chroniques avec comorbidités associées peuvent avoir de nombreuses conséquences psychologiques, sociales et physiques. La prise en charge multidisciplinaire fait appel de façon variable à l’orthophoniste, au psychomotricien, au neurologue, à l’ORL, au dentiste, à l’orthodontiste, au chirurgien maxillo-facial et au gastro-entérologue.
Quelques rappels sur la physiologie salivaire
Fonctions salivaires
Les principales fonctions de la salive sont les suivantes :
– lubrification de la cavité orale et des dents indispensable à l’hygiène bucco-dentaire ;
– effet bactériostatique et bactéricide de certains composants, ainsi que du pH légèrement acide par rapport au pH physiologique (6,5-7,4) ;
– facilitation de la déglutition ;
– début de digestion (amylase, lipase).
Production salivaire
La production quotidienne chez l’enfant avant la puberté est comprise entre 750 à 900 ml/j. Au-delà de cette tranche d’âge, cette production atteint 1 à 1,5 l/j. Soixante-dix pour cent de la salive est sécrétée par les glandes sous-mandibulaires. Cette salive est fluide. Elle représente l’essentiel de la salivation en situation de repos alimentaire. Vingt-cinq pour cent de la salive est produite par les glandes parotides. Il s’agit également d’une salive fluide utile au ramollissement et à l’homogénéisation du bol alimentaire.
La salive sécrétée par les glandes sublinguales (5 % de la production salivaire totale) est épaisse et joue un rôle de protection des dents. La sécrétion salivaire est sous contrôle du système parasympathique pour l’abondance et du système sympathique pour la viscosité. Ces composantes du système nerveux autonome sont elles-mêmes modulées par des stimuli corticaux visuels, olfactifs et gustatifs.
Continence labiale et déglutition salivaire
La continence du sphincter labial est habituellement obtenue vers 15-18 mois, mais un grand nombre d’enfants continuent à baver jusqu’à 3 ans, notamment au moment des repas. La persistance d’un bavage est considérée comme anormale après 4 ans.
La déglutition de salive est un phénomène réflexe faisant intervenir 25 paires de muscles, sous la dépendance de noyaux bulbaires. La fréquence de déglutition salivaire réflexe chez l’adulte est d’une par minute. On ne connaît pas cette fréquence chez l’enfant.
Elle comporte trois temps (oral, pharyngé et œsophagien) et nécessite l’intégrité des systèmes moteurs et sensitifs buccopharyngo-laryngés, et donc des nerfs crâniens concernés (paires V, VII, XII, IX et X).
Hypersalivation et bavage
Définitions et conséquences cliniques
La sialorrhée, hypersialorrhée ou hypersalivation, correspond à un déséquilibre entre les quantités de salive avalées et produites.
La prévalence des hypersialorrhées chroniques de l’enfant est estimée à 0,6 %. Les conséquences les plus fréquentes de l’hypersalivation sont :
– un bavage à l’origine d’un retentissement psychologique et social, d’une irritation de la peau périlabiale et d’infections périorales ;
– une gène à l’élocution ;
– une mauvaise odeur liée à la présence de salive séchée sur la peau et les vêtements.
Un encombrement pharyngé à risque de dyspnée ou de fausses routes, ainsi qu’une déshydratation sont des conséquences plus rares.
Le bavage simple de l’enfant en bas âge sans troubles associés
La cause habituelle de ce bavage est la persistance de la déglutition primaire avec succion au-delà de l’âge de 4 ans. Une déglutition de type primaire peut parfois persister jusqu’à l’âge de 10 ans. Cette situation est favorisée par les tétines, les doudous sucés et la succion du pouce. La musculature labiale demeure hypotonique et la bouche reste ouverte, ce qui entraîne un défaut de scellement des lèvres, à l’origine d’une « incontinence » salivaire, et génère un déséquilibre entre les forces centripètes musculaires labiales et centrifuges linguales.
Ce déséquilibre de forces musculaires, exercé sur les structures dentaire et maxillo-mandibulaire en croissance, contribue à une déformation des mâchoires, avec le développement d’anomalies de l’occlusion dentaire dans le sens vertical ou sagittal : diastèmes, béances (absence de contact entre les incisives), décalages de classes II ou III.
Enfin, toujours du fait de la persistance de cette déglutition primaire, la langue reste en position basse et antérieure et ne stimule pas la croissance du maxillaire, ce qui favorise l’étroitesse du palais et des fosses nasales et donc les gênes respiratoires, notamment durant le sommeil. La prise en charge de ces enfants consiste à essayer de supprimer le facteur entretenant l’habitude de succion (tétine, doudou, pouce).
Si cela ne suffit pas ou en cas d’anomalie occlusive évidente (décalage anormal entre les arcades dentaires inférieure et supérieure ; inclinaisons dentaires anormales visant à compenser ces décalages), le recours à l’orthodontiste devient nécessaire. Celui-ci pourra faire appel à différents types de traitement :
– recours à un kinésithérapeute ou à un orthophoniste pour une rééducation des praxies bucco-linguales (exercices de déglutition, figure 1) ;
– prescription d’appareils appelés écrans vestibulaires buccaux (exemple : écran MuppyTM, Dr. Hinz Dental GmbH & Co, Herne, Allemagne) permettant souvent de supprimer en quelques semaines la déglutition primaire (figure 2) ;
– traitement orthodontique ou plus exactement orthopédique dento-faciale, en cas d’anomalies occlusales, car cette thérapie agit non seulement sur les dents mais aussi et surtout sur leurs bases osseuses maxillo-mandibulaires.
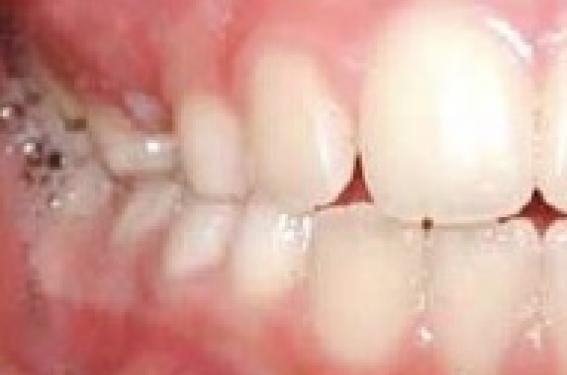
Figure 1. Lucas, 7 ans. Béance dentaire avec pulsion linguale et perlèches
angulaires permanentes par irritation salivaire (A, B, C).
Après traitement par rééducation fonctionnelle et éducateur amovible
(ici une enveloppe linguale nocturne), les dents ont poussé toutes seules,
corrigeant la béance incisive (D), et les lèvres se sont jointes.
Figure 2. Écran vestibulaire buccal Muppy™
(Dr. Hinz Dental GmbH & Co, Herne, Allemagne)
destiné à corriger en quelques semaines les déglutitions primaires persistantes.
L’hypersialorrhée chronique sur un terrain de pathologie chronique sévère
Les principales étiologies et les facteurs aggravants sont résumés dans la figure 3. La première cause d’hypersialorrhée chronique de l’enfant est la paralysie cérébrale (PC) : environ un tiers des enfants atteints d’une PC présentent de tels troubles. Chez l’adulte, l’étiologie la plus fréquente d’hypersialorrhée est la maladie de Parkinson.
Figure 3. Étiologies et facteurs aggravants des hypersialorrhées chroniques.
Le syndrome CHARGE
La première cause d’encombrement pharyngé salivaire chronique chez le petit enfant est le syndrome CHARGE. Dans le cadre de ce syndrome, l’encombrement salivaire est pris en charge en même temps que les troubles respiratoires et de la déglutition par des thérapeutiques invasives : trachéotomie avec éventuelle mise en place d’une canule à ballonnet pour limiter le passage de salive dans les bronches, gastrostomie d’alimentation, chirurgie anti-reflux.
Bilan clinique et paraclinique
La prise en charge d’une hypersialorrhée chronique de l’enfant avec comorbidité associée est multidisciplinaire, faisant intervenir à des degrés variables le pédiatre, l’orthophoniste, le psychomotricien, le neurologue, l’ORL, le dentiste, l’orthodontiste, le chirurgien maxillo-facial ou le gastroentérologue, au mieux dans le cadre de consultations multidisciplinaires. De nombreux éléments sont à analyser.
Il faut en particulier :
• évaluer l’état dentaire, l’hygiène buccale, rechercher des troubles de l’occlusion et une inflammation bucco-pharyngée ;
• rechercher une obstruction nasale ;
• rechercher un reflux gastroœsophagien et un terrain allergique ;
• observer la posture, notamment de la tête ;
• analyser la motricité et la sensibilité faciale, buccale et pharyngée ;
• observer l’enfant manger et boire, à l’état basal et éventuellement lors de l’exécution d’une tâche simple requérant sa concentration. Une analyse plus poussée de la déglutition par fibroscopie ou radiocinéma est parfois indiquée ;
• analyser la parole ;
• pratiquer un examen pédiatrique et neurologique complet ;
• évaluer le retentissement de l’hypersialorrhée à cette fin ; différentes échelles de retentissement du bavage sont utilisables (Reid et coll. 2010)(1) ;
• effectuer un bilan pulmonaire en cas d’encombrement pharyngé, éventuellement associé à des fausses routes.
Prise en charge thérapeutique
Nursing quotidien
Des bracelets sportifs en tissu éponge peuvent être utilisés si l’enfant est capable de s’essuyer la bouche. Des dispositifs plus spécifiques peuvent permettre d’éviter les vêtements trop mouillés. Il convient également d’éviter que l’enfant ne mette trop les doigts dans la bouche car cela stimule la sécrétion salivaire. Ceci peut s’obtenir par des manœuvres distractives utilisant d’autres stimulations sensorielles ou par le port de gants dans les cas les plus sévères. Concernant le nettoyage des lèvres, le tapotement est préférable à l’essuyage car il stimule moins la sécrétion salivaire.
Adaptations diététiques et suppression de traitements médicamenteux aggravants
Afin de diminuer la production salivaire, il convient d’éviter les sodas sucrés pétillants et les aliments acides (citron, vinaigre). Il faut par ailleurs supprimer si possible les médicaments augmentant la production salivaire (benzodiazépines, neuroleptiques, anticholinestérasiques, pilocarpine).
Prise en charge psychologique et rééducative
Une prise en charge par un psychologue peut être très utile pour diminuer le retentissement psychique du bavage si l’âge ou l’état cognitif de l’enfant le permettent.
L’orthophoniste, le psychomotricien et le kinésithérapeute sont impliqués dans la rééducation qui vise à améliorer le contrôle postural de la tête, du cou et du tronc, ainsi que les praxies buccomotrices. Les exercices buccomoteurs permettent d’optimiser le tonus oro-facial, la conscience sensorielle et le contrôle volontaire du mouvement. L’efficacité de ces exercices n’est que peu étayée par des preuves scientifiques, et les résultats sont subjectifs.
Le contrôle obtenu varie selon le niveau de concentration de l’enfant et des autres tâches qu’il est en train d’effectuer. Cette rééducation des praxies buccomotrices nécessite que l’enfant ait un niveau d’attention et d’observance suffisant.
En pratique, elle n’est réalisable que chez des jeunes patients ayant des troubles modérés de la motricité buccolabiale, dotés de capacités cognitives suffisantes et d’un haut niveau de motivation. L’adhérence parentale au programme est essentielle au résultat.
La rééducation peut également faire appel à des techniques de thérapie comportementale ou de biofeedback :
– signal sonore rappelant régulièrement à l’enfant d’avaler sa salive (Domaracki et Sisson, 1990)(2) ;
– placé devant un miroir, le patient doit s’essuyer le visage lorsque ce dernier est mouillé. Une telle technique permet à l’enfant de faire la distinction entre les concepts « mouillé » et « sec ».
Traitement des facteurs bucco-dentaires aggravants
Les caries, gingivites, parodontopathies ou aphtes doivent être traités. Les malocclusions dentaires doivent être corrigées. Des orthèses endobuccales ont été proposées pour lutter contre l’hypersalivation et le bavage. Leurs formes très spécifiques comporte une série de creux et de bosses qui guident le positionnement dentaire et favorisent la fermeture des lèvres. Elles sont également munies d’une rampe pour rediriger la pointe linguale vers le palais. Elles stimulent ainsi les mouvements actifs labiaux, linguaux et vélopalatins (Inga et
coll. 2001)(3). Elles ne sont destinées qu’aux enfants ayant suffisamment de dents (à partir de 2,5-3 ans) et un bavage modéré. Les risques d’inhalation et de blocage dans les voies aériennes supérieures font qu’elles sont contre-indiquées chez les enfants ayant un mauvais contrôle des mouvements linguaux ou en cas d’épilepsie.
Rôles de l’ORL et du gastro-entérologue
L’ORL et le gastro-entérologue prennent en charge les désordres susceptibles d’aggraver l’hypersalivation ou ses conséquences : les hypertrophies adénoïdo-amygdaliennes, rhinites chroniques, allergies ORL et le reflux gastroœsophagien.
Traitements médicamenteux
Les anticholinergiques
Leurs effets secondaires sont fréquents : troubles de l’accommodation visuelle avec vision floue, sécheresse oculaire, sécheresse buccale et épaississement salivaire pouvant aggraver des troubles moteurs bucco-pharyngés, constipation, rétention urinaire, aggravation d’un RGO, effets centraux (sédation, irritabilité, céphalées, augmentation de la fréquence des convulsions). Leurs contre-indications sont le glaucome, la myasthénie, des antécédents de rétention urinaire, l’hypertension artérielle. Leur utilisation dans le cadre des hypersalivations est hors AMM. Les patchs de scopolamine (Hyoscine®) sont plutôt utilisés en Europe. Ils peuvent entraîner des réactions allergiques locales en plus d’effets systémiques. Ils sont assez efficaces à court terme, mais leur effet disparaît sur le long terme.
Dans une étude prospective portant sur 39 enfants, Jongerius et coll. (2004)(4) ont observé 95 % d’efficacité à court terme de ces patchs, mais avec 82 % d’effets secondaires. Ces complications étaient considérées comme bénignes dans 11 % des cas, modérées dans 31 % et sévères dans 40 % des cas. Chez 9 % des patients, la sévérité des effets indésirables a conduit à l’arrêt du traitement (xérostomie : 67 % ; agitation : 36 % ; somnolence : 36 % ; vision floue :20 % ; confusion : 20 %). Le patch est à changer toutes les 48 heures. Avant l’âge de 8 ans, il faut commencer avec un demi-patch puis passer à un patch. Pour obtenir un demi-patch, celui-ci ne doit pas être coupé mais plié en deux (coller la demi-surface ne faisant pas face à la peau à un pansement adhésif).
Deux anticholinergiques oraux sont utilisables, le glycopyrolate (Robinul®) et le trihexyphénidyle (Artane®).
Le glycopyrrolate est l’anticholinergique préférentiellement utilisé dans cette indication aux États-Unis. Sa posologie est de 0,04 mg/kg 3 fois par jour, à atteindre progressivement (Evatt 2011)(5). L’effet débute 15 à 30 min après la prise et dure de 6 à 8 h. Le glycopyrrolate ne franchit pas la barrière hémato-encéphalique et n’entraîne donc pas d’effets centraux. La constipation est constante.
Le trihexyphénidyle se prescrit à la posologie de 2 mg 3 fois par jour, à atteindre progressivement (Reddihough et coll. 1990)(6). Cette molécule est surtout utilisée à doses plus élevées pour réduire la rigidité chez les enfants souffrant de paralysies cérébrales dystoniques.
La toxine botulique A(7,8)
L’injection est réalisée sous anesthésie générale et souvent sous guidage échographique. Elle permet le blocage définitif du relargage de l’acétylcholine au niveau des terminaisons nerveuses, régulant ainsi la sécrétion des glandes salivaires. Cependant, l’effet est temporaire du fait d’une réinnervation secondaire parasympathique. Les principaux risques liés à ce traitement sont :
– la possible aggravation de troubles de la déglutition par épaississement salivaire ou par diffusion du produit vers les muscles bucco-pharyngés. Il faut donc être très prudent dans ses indications et dans la technique (posologie modérée, injections sous guidage échographique) en cas de troubles sévères de la déglutition ;
– des douleurs transitoires, des hématomes, des infections au point d’injection, une augmentation de volume des glandes salivaires. Notons qu’il n’existe aucun risque d’effet systémique en cas de passage sanguin du fait des faibles doses utilisées. Il est possible d’utiliser les injections de toxines botuliques chez des patients aux antécédents de chirurgie des glandes salivaires.
Les protocoles d’administration sont variables. L’injection concerne les deux glandes sous-mandibulaires et éventuellement une ou deux parotides. Les doses sont variables. On pourra proposer, par exemple, avant 8 ans, 5 à 7,5 UI par glande sous-mandibulaire (aliquots : 0,2-0,3 ml) et 3,7 à 5 UI par glande parotide (aliquots : 0,15-0,2 ml), avec une dose maximale totale de 15 à 30 UI. On peut doubler les doses après 8 ans. La surveillance clinique avant le retour à domicile doit être au minimum de 2 h après injection. Durant la semaine post-injection, l’alimentation doit être mixée et il faut contacter la famille par téléphone pour s’assurer de l’absence de troubles de la déglutition ou de difficultés respiratoires.
L’efficacité de la toxine a été démontrée par plusieurs études prospectives randomisées. Elle était en moyenne de 79 % (33-100 %) dans 3 études rétrospectives et 10 études prospectives revues par Khan et coll. en 2011. Ces chiffres varient selon les critères de succès choisis. Ainsi, dans la revue de Khan et coll. (2011)(9), les parents rapportaient 80 % d’amélioration de la qualité de vie de leur enfant mais n’étaient satisfaits du traitement que dans 60 % des cas.
La durée du bénéfice de ces injections est comprise entre 1 et 6 mois (4,5 mois en moyenne) (Khan et coll., 2011)(9). L’effet est maximal 4 à 6 semaines après l’injection. Des réinjections sont possibles, en respectant un délai minimal d’au moins 4 mois entre deux séances. L’apparition d’anticorps antitoxine botulique A est observée dans 3 à 10 % des cas (Khan et coll., 2011) au cours des injections successives(9). On peut alors utiliser la toxine botulique B (Dressler, 2004)(10).
Au total, l’effet transitoire de la toxine botulique A doit conduire à bien choisir le moment pour débuter ce traitement. L’idéal est habituellement l’entrée à l’école car :
– il s’agit d’une étape essentielle dans la socialisation de l’enfant ;
– dans cette tranche d’âge, on peut commencer une rééducation motrice bucco-faciale ou un biofeedback efficace. Le fait de débuter en même temps rééducation et traitement pharmacologique permet à l’enfant de se rendre compte de ce qu’est un menton sec et le place dans une situation de succès qui le motive pour poursuivre sa rééducation.
Chirurgie des canaux et des glandes salivaires(11,12)
Différentes combinaisons de chirurgie des canaux et des glandes salivaires sont possibles parmi les gestes suivants : déroutement ou ligature des canaux de Wharton ou de Sténon ; exérèse des glandes sous-mandibulaires ou sublinguales.
Une métaanalyse de Reed (2009)(12) a étudié 50 articles sur le sujet, triés pour leurs qualités méthodologiques parmi 325 articles lus. Le suivi médian des patients était de 8,1 mois (1-50). D’après cette métaanalyse, 81,6 % des patients ont ressenti une amélioration après la chirurgie, sans qu’il y ait de différences significatives d’efficacité entre les différentes techniques. Le pourcentage de succès le plus élevé (87,8 %) a été rapporté pour la sous-mandibulectomie associée au déroutement des canaux de Sténon et le plus bas (64,1 %) pour la ligature des 4 canaux salivaires, mais seules 4 études ont analysé l’efficacité de cette technique.
Concernant les effets secondaires et complications de la chirurgie, les gestes de ligature des canaux salivaires entraînent un gonflement douloureux de la glande durant une dizaine de jours, rarement des parotidites ou des sous-mandibulites récidivantes. Les gestes touchant à la fois les glandes sous-mandibulaires et les parotides sont à risques majorés de xérostomie pouvant entraîner des caries, des douleurs, des infections locales ou majorer des troubles de la déglutition. Le déroutement des canaux de Wharton a l’avantage de ne pas entraîner de cicatrice cutanée.
Au total, en comparaison des traitements médicamenteux ou de l’injection de toxine botulinique, la chirurgie des glandes et des canaux salivaires est plus invasive et semble d’efficacité comparable. Ses effets sont plus durables, ce qui peut être un avantage en termes d’efficacité ou un désavantage en termes d’effets secondaires (xérostomie, épaississement des sécrétions, majoration des troubles de la déglutition, etc.).
La figure 4 résume les places respectives des différents types de traitement. Notons enfin qu’en cas de fausses routes majeures risquant d’endommager le parenchyme pulmonaire et de mettre en jeu le pronostic vital, une trachéotomie avec mise en place d’une canule à ballonnet, voire une chirurgie d’exclusion laryngée peuvent être nécessaires.
Figure 4. Schéma thérapeutique dans les hypersialorrhées chroniques avec comorbidités associées.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :